限时微模拟(30min)
“3+2”模拟练(一)
一、选择题
1. 下列化学用语或图示表达错误的是()
A. CH3CH(CH2CH3)2的名称:3-甲基戊烷
B. SO2的VSEPR模型: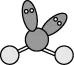
C. CH4中C原子杂化轨道的电子云轮廓图: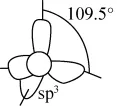
D. CaF2的形成过程: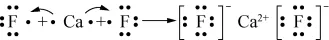
2. 下列实验目的对应的实验操作正确的是()
选项 | 实验目的 | 实验操作 |
A | 检验CH3CH2X中的卤素原子的种类 | 将CH3CH2X(卤代烃)与NaOH溶液共热,冷却后取上层水溶液,加入AgNO3溶液,观察沉淀颜色 |
B | 证明金属活动性:K>Cu | 将少量K投入CuSO4溶液中,观察是否产生红色固体 |
C | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,观察是否有气体生成 |
D | 验证久置的 Na2SO3是否变质 | 取少量久置的亚硫酸钠样品溶于除氧蒸馏水中,加入足量的稀盐酸,再滴加氯化钡溶液,观察是否有白色沉淀出现 |
3. 常温下,用0.100 0mol/L盐酸分别滴定20.00mL浓度均为0.100 0mol/L三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是()
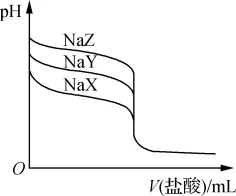
A. 该NaX溶液中:c(Na+)>c(X-)>c(OH-)>c(H+)
B. 三种一元弱酸的电离常数:Ka(HX)>Ka(HY)>Ka(HZ)
C. 当pH=7时,三种溶液中:c(X-)=c(Y-)=c(Z-)
D. 分别滴加20.00mL盐酸后,再将三种溶液混合:c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-)
二、填空题
4. Fe(OH)2具有较强的还原性,新制的白色Fe(OH)2会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色Fe(OH)2,某实验小组做了如下探究实验。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、__________、____________。
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是________________________________________________________。
(3)甲同学按如图a所示操作制备Fe(OH)2(溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:____________________________________________________________________。
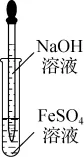
图a
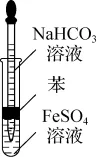
图b
(4)乙同学经查阅资料后设计了如图b所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色Fe(OH)2。
①该反应的原理为__________________________________________________________(用离子方程式表示)。
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:______________________________________________________。(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
c(FeSO4)/(mol/L) | c(NaHCO3)/(mol/L) |
1.0 | 1.5 | 2.0 |
1.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
稳定时间 | 3.5 min | 9 min | 24 min |
1.5 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
稳定时间 | 13 min | 15 min | 22 min |
2.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率加快 | 常温下无现象,加热后产生白色沉淀 |
稳定时间 | 3 min | 8 min | 30 min |
①由以上实验可得到的规律是_____________________________________________。
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为__________(填“1.0”“1.5”或“2.0”) mol/L。
(6)实验创新:延长Fe(OH)2沉淀的稳定时间还可以采取的措施为__________________________________________________________________(任写一条)。
5. 一种合成有机物G的合成路线如图:
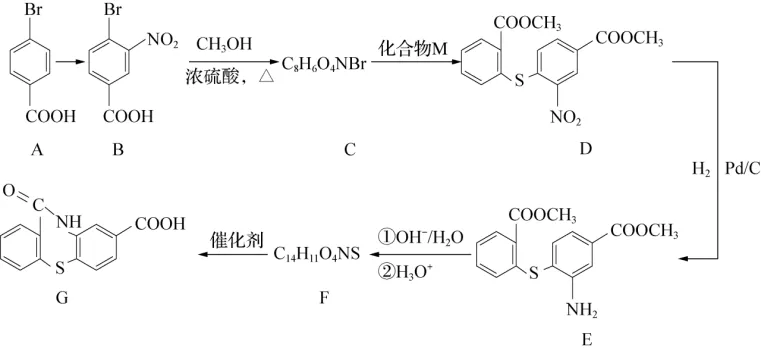
(1)A→B反应的试剂和条件是________________________。
(2)B→C反应的反应类型为__________________________,C中含氧官能团的名称为________________。
(3)M的化学式为C8H8O2S,则M的结构简式为______。
(4)写出反应E→F的化学方程式:______________________
________________。
(5)化合物K是A的同系物,相对分子质量比A的多14。K的同分异构体中,同时满足下列条件,且核磁共振氢谱有5组峰,峰面积之比为2∶2∶1∶1∶1的结构简式为______(不考虑立体异构)。
a.能与FeCl3溶液发生显色反应;b.能发生银镜反应;c.苯环上有2个取代基。
(6)以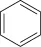 和
和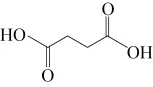 为原料,结合上述合成线路中的相关信息,设计合成
为原料,结合上述合成线路中的相关信息,设计合成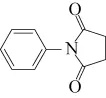 的路线(用流程图表示,无机试剂任选)。
的路线(用流程图表示,无机试剂任选)。
“3+2”模拟练(三)
一、选择题
1. 下列实验操作正确的是()
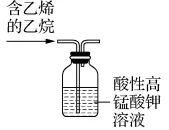
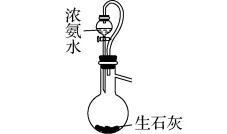
A. 提纯乙烷B. 制备氨气
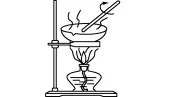
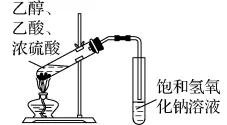
C. 制备无水Na2SO3D. 制乙酸乙酯
2. X、Y、Z、W为短周期的四种元素,原子序数依次增大。X、Y、W三种元素分别位于不同短周期的不同主族。Z、W对应的简单离子核外电子排布相同,X、Y、Z、W元素可形成一种新型漂白剂(结构如图)。下列说法不正确的是()
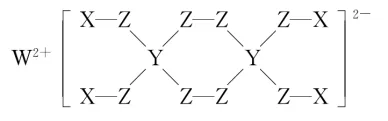
A. 电负性:Z>Y>X>W
B. Y、Z杂化方式相同
C. 1 mol 该化合物的阴离子中含有2 mol 配位键
D. 漂白剂中Z的化合价为-1、-2
3. 甲酸燃料电池工作原理如下图所示,已知该半透膜只允许K+通过。下列有关说法错误的是()
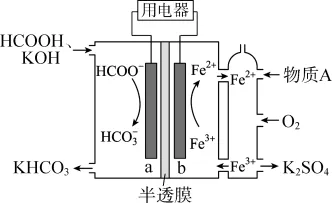
A. 物质A是H2SO4
B. K+经过半透膜自a极向b极迁移
C. a极电极反应式为HCOO-+2e-+2OH-===HCO3+H2O
D. Fe3+可以看作是该反应的催化剂,可以循环利用
二、填空题
4. Ⅰ. 配制100 mL 0.05 mol/L Fe2(SO4)3溶液。
(1)该实验需要用到的玻璃仪器有:烧杯、量筒、玻璃棒、____________、______________________。
(2)为了防止Fe2(SO4)3水解,在配置过程中可以加入少量__________。
Ⅱ.探究Fe2(SO4)3与Cu的反应。
[原理预测] (3)请写出Fe2(SO4)3与Cu的反应的离子方程式:______________________________________________。
[开展实验] 某实验小组在进行Fe2(SO4)3与Cu的反应时观察到了异常现象,决定对其进行进一步的探究。
实验Ⅰ:
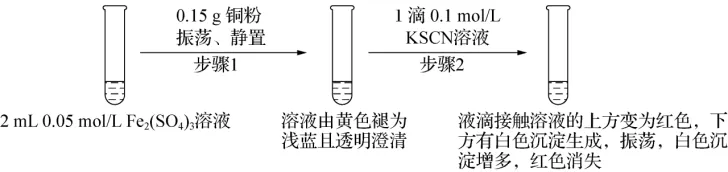
[提出问题] (4)实验前,小组同学预测步骤2后溶液不会变为红色,原因是______________________________________________________________________。
查阅文献:ⅰ.CuSCN为难溶于水的白色固体;
ⅱ.SCN-被称为拟卤素离子,性质与卤素离子相似。
[提出猜想] 经过实验测定白色固体为CuSCN,查阅资料后小组同学猜测CuSCN的生成有如下两种可能。
猜测1:Cu2+与KSCN发生了氧化还原反应。
猜测2:亚铁离子将其还原发生反应:Cu2++Fe2+===Cu++Fe3+、Cu++SCN-===CuSCN↓。
(5)猜测1的离子方程式为______________________________________________________________。
[设计实验]
实验序号 | 对比实验及试剂 | 实验步骤 | 实验现象 |
实验Ⅱ | A试管: 2 mL 0.1 mol/L FeSO4溶液 | 加入1 mL 0.4 mol/L KSCN溶液 | 开始时溶液的上方变为红色,一段时间后红色向下蔓延,最后充满整支试管 |
B试管: 2 mL 0.1 mol/L CuSO4溶液 | 加入1 mL 0.4 mol/L KSCN溶液 | 溶液变成绿色 |
实验Ⅲ | C试管: 2 mL 0.1 mol/L FeSO4溶液 | 加入2 mL 0.1 mol/L CuSO4溶液 | 溶液变为淡蓝色 |
再加1 mL 0.4 mol/L KSCN溶液 | 溶液的上层变为红色,有白色沉淀产生,一段时间后整支试管溶液呈深红色 |
[得出结论] (6)实验Ⅱ中试管______(填字母)中的现象可以证实猜测1不成立。
(7)Fe3+的氧化性本应强于Cu2+,结合实验Ⅲ中的现象解释Cu2++Fe2+===Cu++Fe3+能正向发生的原因:______________________________________________________________________________________________________________________________________。
5. 我国力争于2030年前做到“碳达峰”,2060年前实现“碳中和”,因此CO2的综合利用是研究热点之一。
(1)以CO2为原料可制取甲醇。已知:
Ⅰ. H2(g)、CH3OH(l)的燃烧热ΔH分别为-285.8kJ/mol和-726.5kJ/mol。
Ⅱ. CH3OH(l)CH3OH(g)ΔH=+38kJ/mol
Ⅲ. H2O(l)H2O(g)ΔH=+44kJ/mol
则反应CO2(g)+3H2(g)CH3OH(g)+H2O(g)的ΔH=______________kJ/mol。
(2)利用CO2与H2合成甲醇涉及的主要反应如下:
Ⅰ. CO2(g)+3H2(g)CH3OH(g)+H2O(g)ΔH1
Ⅱ. CO2(g)+H2(g)CO(g)+H2O(g)ΔH2=+41kJ/mol
一定条件下向某刚性容器中充入物质的量之比为1∶3的CO2和H2发生上述反应,在不同催化剂(Cat1,Cat2)下经相同反应时间,CO2转化率和甲醇的选择性[甲醇的选择性=n(CO)+n(CH3OH)×100%]随温度变化如图甲所示。
①由图可知,催化效果Cat1______(填“>”“<”或“=”)Cat2。
②在210~270℃间,CH3OH的选择性随温度的升高而下降,可能原因为______________________________________________________________________________________________________________。
③某条件下,达到平衡时CO2的转化率为15%,CH3OH的选择性为80%,则H2的平衡转化率为__________;反应Ⅱ的平衡常数Kp=______(列出算式即可)。
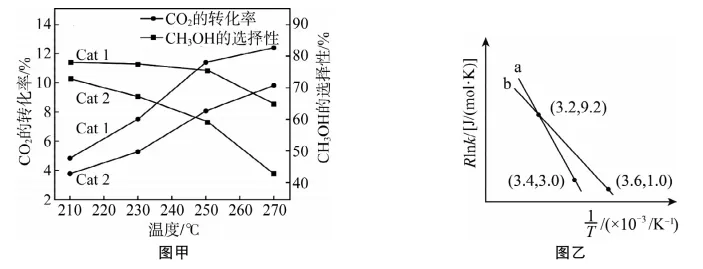
(3)利用制备的甲醇可以催化制取丙烯,过程中发生如下反应:3CH3OH(g)===C3H6(g)+3H2O(g)。该反应的实验数据遵循Arhenius经验公式,如图乙中曲线a所示,已知Arthenius经验公式为Rlnk=-T+C(Ea为活化能,假设受温度影响忽略不计,k为速率常数,R和C为常数),则反应的活化能为________kJ/mol。当改变外界条件时,实验数据如图乙中的曲线b所示,则实验可能改变的外界条件是________________________;此经验公式说明对于某个基元反应,当升高相同温度时,其活化能越大,反应速率增大得________(填“越多”或“越少”)。
▲点击上方 小初高学习资料大全
在公众号消息框发送:
7243,即可免费领取